整理丨山山 共計 17? 條簡訊?|?建議閱讀時間 1 分鐘 ◆??◆??◆ + 政策簡報 86個器械獲批 近日,國家藥監局發布《國家藥監局關于批準注冊86個醫療器械產品公告(2020年9月)(2020年第113號)》。其中,境內第三類醫療器械產品53個,進口第三類醫療器械產品16個,
整理丨山山
共計 17 條簡訊 | 建議閱讀時間 1 分鐘
◆ ◆ ◆
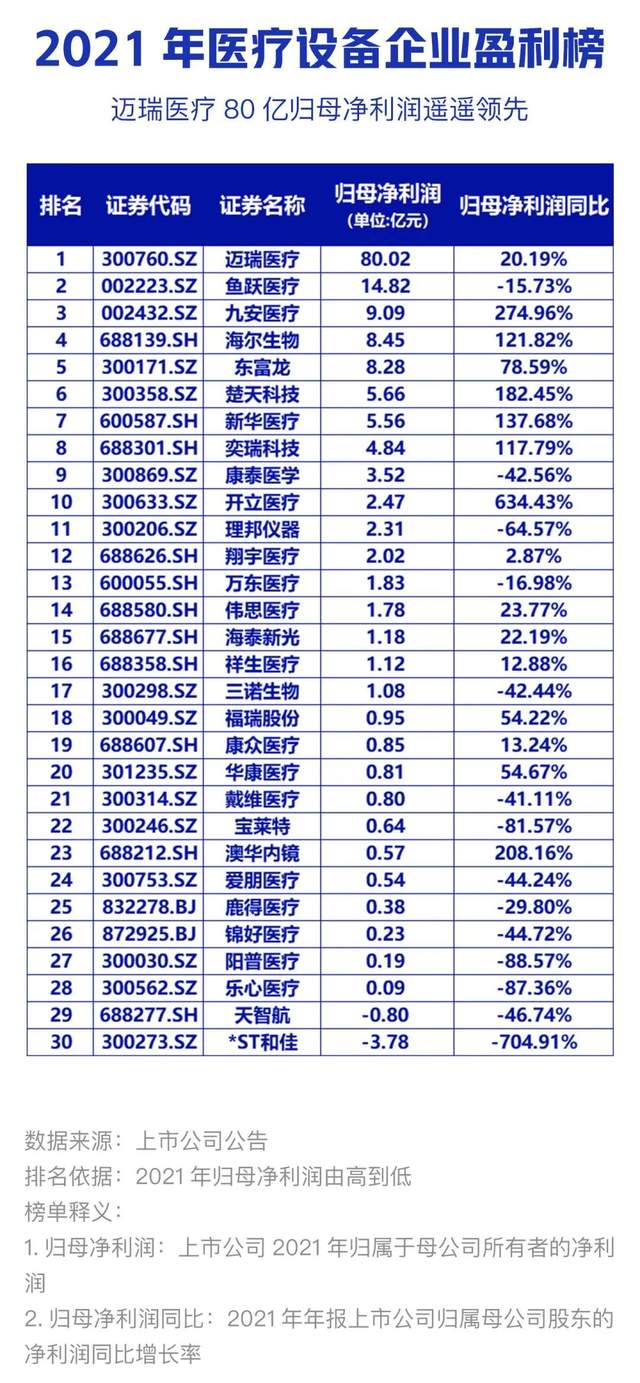
86個器械獲批
Retrophin以5.17億美元收購Orphan獲得新型酶替代療法
日前,Retrophin正以9000萬美元的現金收購Orphan Technologies。Orphan公司擁有尚處研究階段的新型酶替代療法OT-58,將有資格獲得高達4.27億美元的里程碑付款以及中等單位數增長的特許權使用費。(新浪醫藥新聞)
東京大學和衛材宣布合作靶向蛋白質降解技術開發和新藥研發
東京大學與衛材近日宣布,已創建一個針對靶向蛋白質降解技術開發和新藥研發的合作項目,并設立社會合作項目“發現蛋白質降解藥物”。研究時間跨度為五年,從2020年10月1日到2025年9月30日。(美通社)
臻和科技成功完成超人民幣十億元E輪融資
今日,腫瘤精準診療服務企業臻和科技宣布完成金額超人民幣十億元的戰略融資。本輪融資將用于進一步加強臻和腫瘤精準診斷產品的研發創新和引進,加快其IVD產品的注冊申報。(美通社)
衛材和生化學簽訂骨關節炎治療劑SI-613在韓國聯合上市協議
衛材和生化學近日宣布,兩家公司已就生化學首創的骨關節炎治療劑SI-613(雙氯芬酸結合透明質酸鈉)在韓國的聯合上市簽訂協議。這是自衛材和生化學于2020年4月1日就SI-613在中國的共同開發和聯合上市簽署協議以來,締結聯合上市協議的第二個國家。(美通社)
AavantiBio公司剛成立就獲超1億美元融資
10月23日,AavantiBio公司完成1.07億美元A輪融資,并宣布公司成立,參與本輪融資的包括Perceptive Advisors、Bain Capital、RA Capital等投資機構。AavantiBio公司將致力于開發創新性基因療法來治療罕見病,目前開發的基因療法主要針對弗里德希氏共濟失調。(創鑒匯)
泛生子與艾沐蒽簽訂全球獨家許可
10月22日,泛生子宣布與杭州艾沐蒽簽訂獨家許可協議,獲得其血液腫瘤微小殘留病產品的全球獨家許可,并將加速產品開發和商業化。根據協議,泛生子將擁有使用艾沐蒽的Seq-MRD?技術進行研發、注冊、商業化血癌MRD檢測產品的專有權。(藥渡)
默沙東、輝瑞2款肺炎疫苗在歐洲市場出現緊缺
據路透社報道,由于研究人員嘗試使用兩種肺炎球菌疫苗作為預防COVID-19的預防措施,默沙東公司的Pneumovax 23和輝瑞的Prevnar 13在歐洲市場面臨短缺的困境。(新浪醫藥新聞)
阿斯利康Farxiga3期試驗顯著降低CKD患者腎功能惡化、死亡風險
10月23日,阿斯利康公布了突破性3期臨床研究DAPA-CKD的一項新的亞組分析結果,數據表明,在標準護理的基礎上,Farxiga降低了無論根本病因為何的慢性腎病患者發生腎功能惡化或心血管、腎病死亡的風險。(新浪醫藥新聞)
阿斯利康Trixeo Aerosphere在歐盟即將獲批
阿斯利康近日宣布,歐洲藥品管理局CHMP已發布一份積極審查意見,推薦批準美國FDA已批準Trixeo Aerosphere用于慢性阻塞性肺病患者的維持治療。Trixeo Aerosphere是一款三聯療法,在日本、中國、美國被批準以品牌名Breztri Aerosphere上市銷售,用于COPD患者的維持治療。(生物谷)
非小細胞肺癌患者疾病控制率達96%
今日,Mirati公布了其KRAS G12C抑制劑adagrasib(MRTX849)的最新臨床試驗結果,其中包括潛在注冊性2期臨床試驗的數據。試驗結果顯示,在治療接受過化療和一種PD-1/PD-L1抑制劑療法的NSCLC患者時,adagrasib作為單藥療法,達到45%的ORR和96%DCR。(藥明康德)
Revolution公布SHP2+MEK抑制劑最新中期數據
10月24日,Revolution Medicines公布了SHP2抑制劑RMC4630聯和MEK抑制劑考比替尼針對攜帶RAS信號通路改變腫瘤患者的Ⅰb/Ⅱ期研究最新中期數據。數據表明,間歇性RMC-4630與每日或間斷的考比替尼聯合給藥具有可接受的耐受性。該組合將進一步在II期推薦劑量和給藥方案上評估對RAS激活腫瘤中的抗腫瘤活性。(醫藥魔方)
信達生物新型LAG-3/PD-L1雙抗獲批臨床
今日,CDE最新公示,信達生物申報的1類生物新藥IBI323獲得臨床試驗默示許可,擬開發用于治療晚期惡性腫瘤。根據公開資料,IBI323是一款新型LAG-3/PD-L1雙特異性抗體,具有成為“first-in-class”新藥的潛力。(醫藥觀瀾)
恒瑞醫藥兩款1類新藥獲批臨床
今日,CDE最新公示,來自恒瑞醫藥的兩款1類新藥獲得多項臨床試驗默示許可,分別為2型糖尿病候選藥SGLT2抑制劑脯氨酸恒格列凈,以及可增加血小板生成的TPO-R激動劑海曲泊帕乙醇胺片。值得一提的是,兩款1類新藥均已于今年在中國申報新藥上市申請,其中海曲泊帕乙醇胺片還以符合附條件批準被納入優先審評。(醫藥觀瀾)
達石藥業首個IND申請獲受理
10月22日,CDE公示顯示,達石藥業1類生物新藥DS002注射液臨床試驗申請獲得受理。根據公開信息,這是達石藥業遞交的首個IND申請,候選藥物DS002是一種靶向NGF的人源化重組單克隆抗體藥物,擬開發作為無成癮性鎮痛藥。(藥明康德)
Cell子刊:研究發現抗骨質疏松藥新靶標
近日,我國同濟大學岳銳教授課題組在《Cell Reports》上發表最新研究,他們發現了一種成骨抑制因子即成纖維細胞活化蛋白,抑制其活性可以促進骨生成并抑制骨吸收,是治療骨質疏松癥的新型潛在藥物靶標。(生物探索)
鄭州大學發現釋放大量鈣離子可殺死耐藥腫瘤細胞
腫瘤細胞通常通過促進它們自身產生將藥物泵出細胞的蛋白來獲得多藥耐藥性,從而使得化療無效。如今,在一項新的研究中,來自中國鄭州大學的研究人員開發出可以在腫瘤細胞內釋放出大量的鈣離子、抑制藥物泵和逆轉多藥耐藥性的納米顆粒。(生物谷)
2020年Q4十余款新藥有望獲批上市,涉及賽諾菲、輝瑞、BMS
編譯 | newborn 投稿郵箱:yiyao@yidu.sinanet.com ◆ ??◆??◆ 美國著名醫療健康資訊網站Xconomy近日發表文章指出,預計在年底前,將有一批新產品獲得監管批準進入市場,包括賽諾菲、輝瑞、百時美施貴寶的新藥項目,這些藥物上市后,將開辟新的商業領域或動...
本文來源:新浪醫藥 作者:sinayiyao 免責聲明:該文章版權歸原作者所有,僅代表作者觀點,轉載目的在于傳遞更多信息,并不代表“醫藥行”認同其觀點和對其真實性負責。如涉及作品內容、版權和其他問題,請在30日內與我們聯系
 客服微v信:
客服微v信:







 京公網安備 11010802031568號
京公網安備 11010802031568號

